flowchart LR A[Drug delivery systems] --> B(Diffusion Controlled Delivery Devices) B --> B1[Monolithic Devices ] B --> B2[Membrane Controlled Devices ] B --> B3[Swelling-Controlled Devices] B --> B4[Osmotic Pressure Devices] B2 --> C1[Biodegradable polymeric matrices] B2 --> C2[Biodegradable polymeric matrices] B1 --> C1 B1 --> C2
Viên nén đặc biệt và dạng bào chế hiện đại
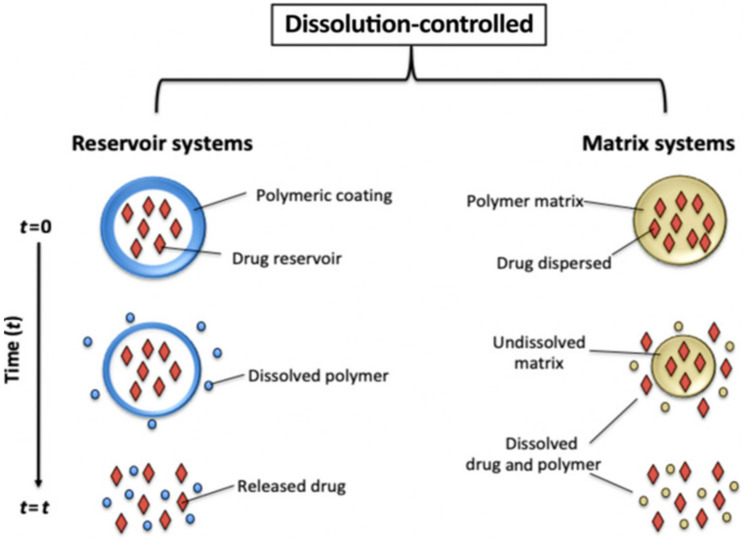
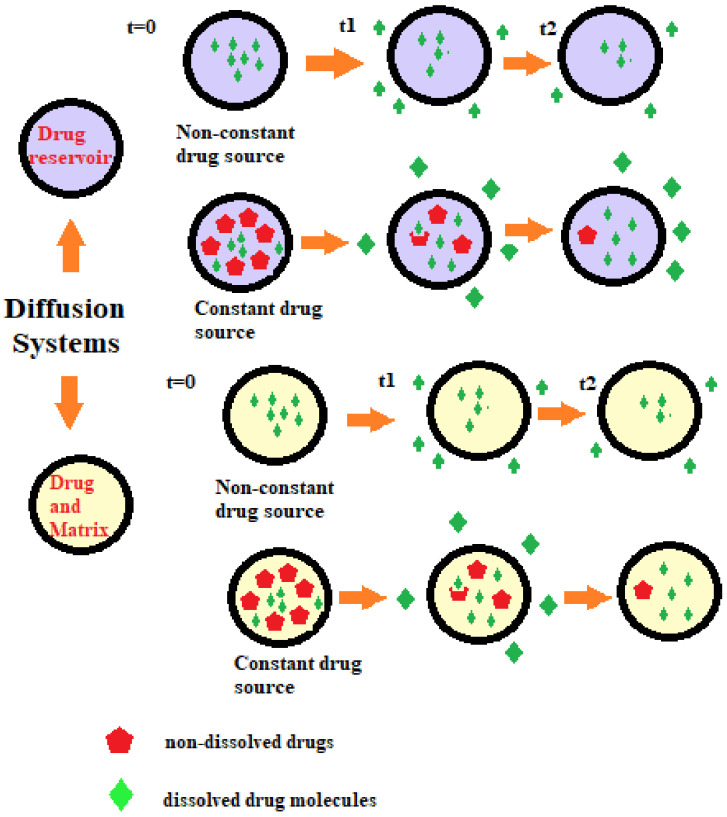
Các hệ thuốc giải phóng kiểm soát nồng độ dược chất theo thời gian
2025-03-14
MỤC TIÊU:
- Trình bày được đặc điểm thành phần, cấu trúc kỳ thuật bào chế, cơ chế giải phóng dược chất từ các hệ thuốc màng bao, hệ cốt, hệ bơm thẩm thấu.
- Phân tích và so sánh được đặc điểm động học quá trình giải phóng được chất từ các hệ thuốc, các yếu tố ảnh hưởng.
- Vận dụng được kiến thức để giải thích vai trò từng thành phần trong công thức thuốc của một số chế phẩm thuộc hệ giải phóng kiểm soát, nguyên tắc bào chế, cơ chế giải phóng dược chất từ hệ thuốc có công thức tương ứng.
Đại cương
| Màng bao | Cốt | Bơm thẩm thấu | |||
|---|---|---|---|---|---|
| Kỹ thuật sản xuất liên quan | |||||
| Viên nén | X | X | X | X | X |
| Viên nang | X | ||||
| Pellet | X | X | X | X | |
| Hỗ dịch | X | ||||
| Nhũ tương | X | ||||
| Hệ trị liệu qua da | X | ||||
| Vi nang | X | X | X | X | |
| Hoạt chất | |||||
| Đô tan trong nước | Dạng muối dễ tan nước hoặc đã làm tăng độ tan | Dễ tan và ít tan | |||
| Độ tan hoạt chất trong polymer | Phân tán | ||||
| Polymer | |||||
| Trong dịch sinh học | Không phân hủy sinh học | Phân hủy sinh học | Không phân hủy sinh học | Phân hủy sinh học | Kết hợp |
| Độ tan trong nước |
Không tan trong nước, tan trong dun mỗi hữu cơ |
Polymer thân nước, trương nở trong nước tạo gel |
Không tan trong nước | Trương nở trong nước | |
| Ví dụ | EC | HPMC | EC | HPMC | CAB |
| polymethacrylat | HPC | PVC | agar | CTA | |
| Zein | sáp | gôm | |||
| alcol béo | alginat | ||||
| aci béo | chitosan | ||||
| Tinh bột biến tính | |||||
| Tá dược khác | |||||
| Tá dược dành cho nhân | Nhân đạt tiêu chuẩn để bao |
Vô cơ: dicalci phosphat, calci sulphat Sơ nước bị ăn mòn sáp, alcol béo, các acid béo |
Tá dược thẩm thấu, Tá dược trương nở, Tá dược trơn, Tá dược tạo kênh |
||
|
Tá dược bào ngoài polymer |
Chất hóa dẻo, chất tạo màu, tạo đục |
Tá dược rắn không tan như TiO2, Talc, Megnesi stearat |
Không có |
màng bán thấm, tá dược tạo lỗ xốp, Dung môi bao, chất hóa dẻo |
|
| Giải phóng | |||||
| Cơ chế giải phóng | Khuếch tán qua màng | Khuếch tán trong màng sau đó là hòa tan | Khuếch tán hoặc ăn mòn |
Khuếch tán với hợp chất dễ tan và ăn mòn với hợp chất khó tan |
|
| Mô hình giải phóng | Bậc 0 | Không theo bậc 0 | Mô hình higuchi | Mô hình noyes-whitney | |
| Bậc 1 | |||||
| Mô hình khác | |||||
Membrane Controlled Devices
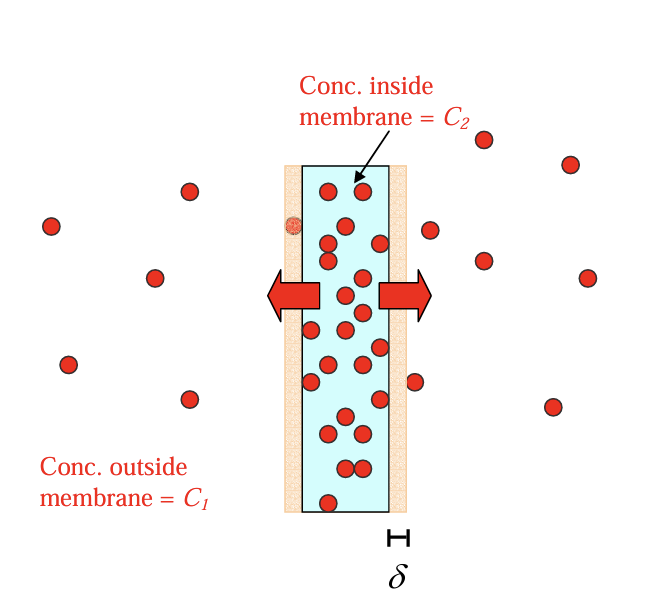
Hệ thuốc màng bao không tan kiểm soát giải phóng hoạt chất
Cấu trúc hệ thuốc
Được bao lớp màng kiểm soát giải phóng. Lớp màng polymer không tan trong dịch sinh học kiểm soát giải phóng dược chất dựa trên các kênh khuyếch tán được tạo ra trong lớp bề dày của màng khi tiếp xúc trực tiếp với môi trường sinh học.
Tốc độ giải phóng
\[\frac{Q}{t}=\frac{K_{m/h} K_{n/m} D_d D_m}{K_{m/h} D_m h_d + K_{n/m} D_d h_m} C_h\] Trong đó:
- \(K_{m/h}\) Hệ số phân bố phân tử dược chất tử hệ thuốc vào màng kiểm soát
- \(K_{n/m}\) Hệ số phân bố phân tử dược chất tử màng kiểm soát vào lớp khuếch tán trong môi trường nước
- \(D_d\) Hệ số khuếch tán trong lớp khuếch tán ở vùng môi trường nước bên ngoài bao quanh màng
- D_m Hệ số khuếch tán dược chất trong mảng
- h_d Bề dày lớp khuếch tán
- h_m Bề dày mảng kiểm soát
- C_h Nồng độ được chất trong hệ thuốc
Thành phần hệ thuốc
Dược chất: dạng muối dễ tan trong nước hoặc được cải thiện độ tan nhờ tạo hệ phân tán rắn, tạo dẫn chất, thêm chất diện hoạt
Tá dược: Avicel, lactose hay muối carbonat không tan tạo kênh dẫn nước. Dược chất có thể tạo pellet, hạt
Màng bao: non-degradable polymeric matrices
- polymer tạo màng thường không tan trong nước
- EC(Ethyl cellulose): EC thường phối hợp với HPMC, PEG. Pha sẵn như Aquacoat ECD
- Polymethacrylat: Eudragit RS, Eudragit RL, eudragit NE
- Chất hóa dẻo
- Chất màu
- Chất tạo đục TiO2, talc
Mô hình giải phóng
Theo định luật Fick:
\[\frac{d_Q}{d_t}= \frac{D(C_-C_t)S}{h_m}\] Trong đó:
- \(C_t\) Là nồng độ dược chất trong môi trường sinh học được cơ thể hấp thu lấy đi tạo nồng độ tối thiểu hằng định
- \(S\) Diện tích bề mặt màng bao không tan sau khi đã trương nở tạo kênh khuếch tán không thay đổi
- \(h_m\) Bề dày màng bao không tan khi đạt cân bằng (cũng như diện tích màng) không thay đồi
- D Hệ số khuếch tán phụ thuộc vào bản chất của dược chất và của màng không thay đổi
| Tá dược | Khối lượng (mg/ml) |
|---|---|
| Diltiazem hydroclorid | 200 mg |
| Avicel pH 102 | 27 mg |
| Lactose monohydrat | 21 mg |
| HPMC E6 | 4 mg |
| Khí dung | 2 mg |
| Nước tinh khiết | 0,12 ml |
Thành phần màng bao pellet giải phóng kiểm soát
| Tá dược | Khối lượng (mg/ml) |
|---|---|
| Eudragit RS 100 | 334,7 mg |
| Magnesi stearat | 5,8 mg |
| Trietyl citrat | 2,0 mg |
| Titan dioxyd | 14,4 mg |
| Talc | 12,0 mg |
| Ethanol | 0,87 ml |
Vỏ nang cứng
| Tá dược | Khối lượng |
|---|---|
| Vỏ nang cứng | 1 vò |
| Tá dược | Khối lượng (mg) |
|---|---|
| Pseudoephedrin hydroclorid | 60 |
| Tinh bột mỳ | 30 |
| Lactose | 190 |
| PVP K30 | 10 |
| Ethanol 70% | 50 |
| Magnesi stearat | 1.5 |
| Bột talc | 3 |
| Aerosil | 1.5 |
Công thức màng bao nhân (kiểm soát giải phóng kéo dài)
| Tá dược | Khối lượng |
|---|---|
| Zein | 2,7 mg |
| Dietyl phtalat | 1 mg |
| Bột talc | 2,5 mg |
| TiO2 | 1 mg |
| Isopropanol - nước (8:2) | 400 ml |
Công thức lớp bao ngoài cùng giải phóng ngay
| Tá dược | Khối lượng (mg/ml) |
|---|---|
| Pseudoephedrin hydroclorid | 60.0 mg |
| Loratadin | 5.0 mg |
| HPMC E6 | 25.0 mg |
| Khí dung | 4.5 mg |
| Talc | 4.5 mg |
| Ethanol 90% | 450 ml |
Màng đặt nhãn khoa giải phòng kiểm soát (Ousert)
Thành phần lớp giữa – hệ chứa dược chất (dày 305 µm)
| Tá dược | Khối lượng (mg) |
|---|---|
| Pilocarpin | 38 |
| Titan dioxyd | 5 |
| Alginat Natri | 200 |
Thành phần 2 lớp màng kiểm soát giải phóng (lớp trên và lớp dưới mỗ μm)
| Tá dược | Khối lượng (mg) |
|---|---|
| Ethylen vinyl axetat | 80 |
Màng hình oval rông 5.7 m dài 13.4 mm tốc độ giải phóng dược chất 20 ug trong một giờ kéo dài trong 7 ngày
Hệ màng bao hòa tan ăn mòn kiểm soát giải phóng dược chất
Cấu trúc hệ thuốc
Hệ thuốc chứa dược chất được bao màng polymer chậm hòa tan bị mòn dần trong môi trường dịch sinh học, màng polymer thân nước trương nở gel tạo ra hàng rao kiểm soát làm chậm và kéo dài quá trình giải phóng. Màng bao có thể có độ dày mỏng khác nhau: 1 lớp bao ngoài hệ chứa dược chất hoặc bao từng lớp màng xen kẽ lớp dược chất tọa ra sự giải phóng ngắt quãng.
Thành phần
Tá dược bao hòa tan mòn dần:
- polymer thân nước: HPMC, HPC
- Tá dược rắn không tan như tio2, Talc, Megnesi stearat
Mô hình dược động học ảnh hưởng bởi độ dày, hệ số phân bố, hệ số khuếch tán.
Mô hình thường bậc 1 hoặc mô hình khác trừ bậc 0
Chủ yếu thuốc giải phóng liều nhắc lại, không dùy trì được nồng độ thuốc hằng định trong máu, có hiện tượng đỉnh và đáy.
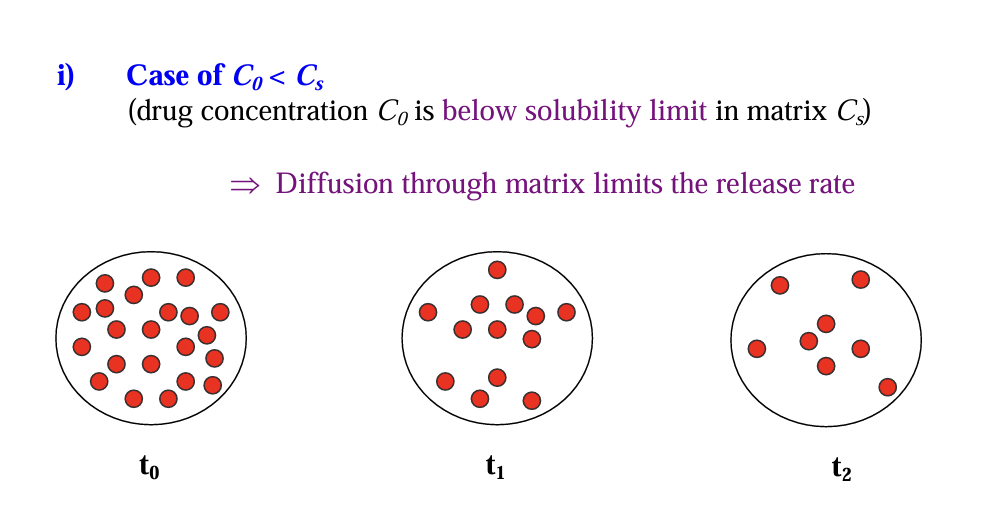
Monolithic Devices
Hệ thuốc cốt không tan kiểm soát giải phóng dược chất
Cấu trúc hệ thuốc
Dược chất phân tán trong cốt không tan trong môi trường sinh học. Cốt đóng vai trò như khung giá mang thuốc. Sau khi tiếp xúc với nước của môi trường, dược chất được hòa tan trong các kênh nước được tạo ra trong cốt và khuyếch tán giải phóng ra khỏi hệ thuốc. Cốt sơ nước có thể bị ăn mòn trong đường tiêu hóa để giải phóng dược chất.
Thành phần
Dược chất là dẫn chất hoặc muối dễ tan. Dược chất có thể hòa tan trong dung môi thích hợp trước khi phân tán vào cốt.
Tá dược là polymer không tan trong nước như ethyl cellulose, poly vinyl chlorid Một số tá dược vô cơ như dicalci phosphat, calci sulphat.
Tá dược sơ nước bị ăn mòn trong đường tiêu hóa dưới tác dụng của hệ enzyme bao gồm sáp, alcol béo, các acid béo
Trong cả 2 hệ cốt nêu trên có thể có các tà dược rắn không tan nhưng thân nước, thấm nước để tạo kênh dẫn nước vào hệ, tham gia điều chỉnh tốc độ giải phóng được chất như Avicel, calci carbonat, dicalci phosphat…
Mô hình higuchi
\[W = (2.C_s.D_m.C_0.t)^{1/2}\]
Trong đó:
- W – Lượng dược chất khuếch tán qua 1 đơn vị diện tích màng tại thời điểm
- \(C_s\) - Độ tan của dược chất
- \(C_0\) – Tổng lượng dược chất có trong 1 đơn vị thể tích cốt
- \(D_m\) – Hệ số khuếch tán trong cốt
Nang cứng salbutamol giải phóng kéo dài
| Tá dược | Khối lượng (mg/%) |
|---|---|
| Salbutamol sunfat | 9.6 mg |
| Sáp ong | 44.0 mg |
| Sáp carnauba | 22.0 mg |
| Avicel PH 101 | 17.0 mg |
| Dicalci photphat | 60.0 mg |
| Magnesi stearat | 1% |
Hệ thuốc giải phóng kiểm soát cốt thân nước hòa tan
Cấu trúc hệ thuốc
Dược chất được phân tán trong cốt thân nước, trương nở hòa tan mòn dần trong môi trường sinh học trong quá trình giải phóng dược chất thành phần
Thành phần
Dược chất: dễ tan trong nước
Tá dược: HPMC hoặc kết hợp, HPMC dòng K và E
Sự giải phóng được chất xảy ra qua các giai đoạn: nước trong môi trường thẩm vào hệ cốt làm cốt trương nở tạo gel, sau đó dược chất hòa tan trong nước có trong hệ cốt đã trương nở, khuếch tán ra môi trường qua hàng rào kiểm soát là lớp gel, đồng thời được giải phóng ra môi trường khi lớp gel bị hòa tan ăn mòn dần.
phương trình Noyes-Whitney
\[ \frac{d_c}{d_t}=\frac{A(C_s-C_t)D}{h}\] de A. (CC). D d h$$
Trong đó:
- \(d_c\) – Tốc độ giải phóng dược chất
- A - Diện tích bề mặt tiếp xúc của hệ với môi trường hòa tan
- \(C_s\) – Nồng độ được chất bão hỏa
- \(C_t\) Nồng độ được chất trong môi trường tại thời điểm t
- D – Hệ số khuếch tán của dược chất trong môi trường hòa tan
- h – Bề dày lớp khuếch tán
- Viên nén felodipin 5mg giải phóng kéo dài
- Viên nén Glipizid 10mg giải phóng kéo dài
- Viên nén Indapamid 1,5mg giải phóng kéo dài
Công thức viên chưa bao (cho 1 viên) :
| Tá dược | Khối lượng (mg) |
|---|---|
| Hệ phân tán rằn Felodipin 10% (Felodipin 10%, PEG 4000 20%, PVP K30 40%, poloxamer 30%) | 50 |
| HPMC E4M | 58 |
| HPMC E151V | 17 |
| Lactose | 87 |
| Magnesi stearat | 2 |
| Bột talc | 1 |
Công thức màng bao bảo vệ (cho 2,15 kg viên = 1000 viên):
| Tá dược | Khối lượng (g) |
|---|---|
| HPMC E6 | 43.0 |
| HPMC E15 | 43.0 |
| PEG4000 | 12.9 |
| Titan dioxyd | 10.8 |
| Câu chuyện | 32.3 |
| Ethanol 96% | 1176 |
| Nước tinh khiết | 392 |
Công thức viên (cho 1 viên):
| Tá dược | Khối lượng (mg) |
|---|---|
| Glipizid | 10 |
| HPMC K4M | 32 |
| HPMC K100LV | 47 |
| Lactose | 78 |
| Aerosil | 1 |
| PVP | 14 |
| Ethanol 90% | vừa đủ |
Màng bao bảo vệ:
| Tá dược | Khối lượng (mg) |
|---|---|
| HPMC E15 | 8.0 |
| PEG6000 | 1.2 |
| Axit stearic | 0.8 |
| Bột talc | 1.2 |
| Ethanol: Nước (2:1) | vừa đủ |
Công thức viên (cho 1 viên):
| Tá dược | Khối lượng (mg) |
|---|---|
| Indapamid | 1.5 |
| HPMC K15M | 98 |
| HPMC E15LV | 10 |
| Poloxamer | 15 |
| Lactose | 33 |
| Dicalci photphat | 30 |
| Magnesi stearat | 2 |
| Khí dung | 1 |
| PVP K30 | 10 |
| Ethanol 96% | vừa đủ |
Công thức màng bao bảo vệ (cho 2,0 kg viên):
| Tá dược | Khối lượng (g) |
|---|---|
| HPMC E6 | 40 |
| HPMC E15 | 40 |
| PEG4000 | 12 |
| Titan dioxyd | 10 |
| Bột talc | 30 |
| Ethanol 96% | 1094 |
| Nước tinh khiết | 364 |
Osmotic Pressure Devices
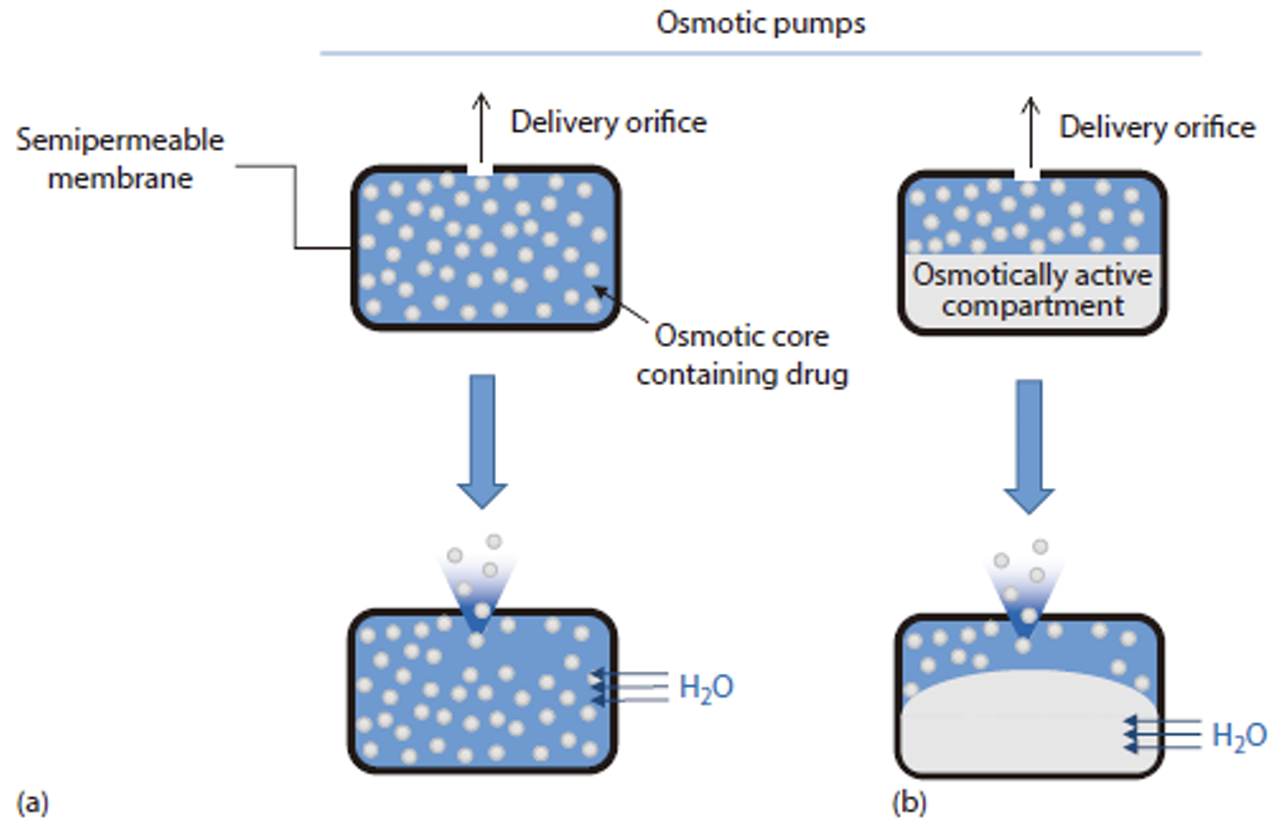
Hệ thuốc bơm thẩm thấu giải phóng kiểm soát
Cấu trúc hệ thuốc
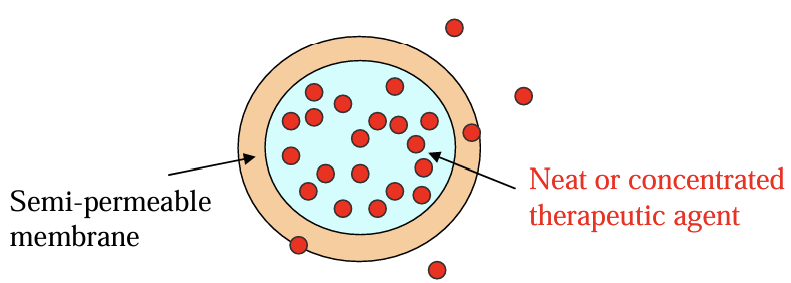
Dược chất được bao trong một màng bao bán thấm có lỗ giải phóng dược chất. Màng này chỉ cho dung môi thấm vào hòa tan dược chất. áp suất thẩm thấu tạo ra trong hệ là động lực đẩy dung dịch dược chất qua miệng giếng giải phóng dược chất.
Hệ bơm thẩm thấu 1 ngăn
- Hệ bơm thẩm thấu quy ước: Nước qua màng bán thấm vào trong thuốc, dược chất hòa tan tạo ra dung dịch có áp suát thẩm thấu lớn trong hệ, dung dịch dược chất được bơm đẩy ra môi trường sinh học dựa trên các lô giải phóng dược chất đến khi cân bằng áp suất trong ngoài màng.
- Hệ thơm thẩm thấy tự tạo lỗ xốp: Nước tiếp xúc màng bao, hòa tan các chất tan là tá dược tạo lỗ xốp trong bằng bao, tạo hệ vi lỗ. Nước qua màng bán thấm và vi lỗ xốp vào trong hệ hòa tan dược chất và chất tan có trong hệ thuốc tạo áp suất thẩm thấu lớn. Dung dịch được bơm đẩy ra môi trường qua hệ vi miệng lỗ giải phóng đên skhi cần.
Hệ bơm thẩm thấu 2 ngăn
- Hệ bơm thẩm thấu kéo-đẩy: Nước thẩm thấu, hòa tan dược chất tạo dịch, gây trương nở tá dược polymer làm lớp đẩy. Dung dịch thuốc giải phóng ra khỏi thuốc dựa trên áp suất tạo ra trong hệ do trương nở polymer và áp suất thẩm thấu
- Hệ bơm thẩm thấu kiểu sandwich: tương tự kiểu kéo đẩy nhưng lớp đẩy nằm giữa hai lớp hoạt chất.
- Hệ bơm thẩm thấu lỏng: hệ thuốc dược chất lỏng thân dầu hoặc dung dịch dầu có thêm chất như hóa đóng trong nang mềm hoặc nang cứng. Nước thấm thấm qua màng vào trong, nước hòa tan dược chất dễ tan tạo ra áp suất thẩm thấu. dược chất lỏng hoặc dung dịch đẩy nhờ áp suất trong hệ qua miện lỗ giải phóng.
Cơ chế với hệ thuốc lỏng
\[\frac{Q}{t} = \frac{P_n A_m}{h_m} (\delta\pi - \delta P)\]
Trong đó:
- \(P_n\) - Độ thấm nước qua màng.
- \(A_m\) – Diện tích bề mặt màng thẩm thấu hiệu dụng (có hiệu qua thâm thầu).
- \(h_m\) - Độ dày của màng.
- \(\delta\pi\) và \(\delta P\) – chênh lệch áp suất thẩm thấu và chênh lệch áp suất thủy động trong và ngoài màng.
- \(C_s\) - Độ tan trong nước của dược chất chứa trong hệ thuốc răn.
Dược chất: bệnh mạn tính như nifedipin, glipzid, famotidin, tramadol, carbamazepin, diliazem, metoprolol
Tá dược cốt:
- Tá dược thẩm thấu: muối vô cơ như natri clorid, kali clorid, muối natri kali sulfat hoặc carbonat, các loại đường như glucose, sorbitol, sucrose
- Tá dược trương nở: polymer hút nước như tinh bột biến tính, crossarmelose, cellulose vi tinh thể, carbopol, HPLC, NaCMC
- Tá dược trơn: Magesi stearat, titan dioxd, aerosil, bột talcs
- Tá dược tạo kênh: có thể trương nở hoặc không trương nỏ: kaolin, silic dioxyd, natri lauryl sulfat, polyvinyl pryrrrolidon, bentonit, polyester,
- Thành phần tạo màng:
- màng bán thấm: cellulose acetatm cellulose acetat butylra, cellulose triacetat
- tá dược tạo lỗ xốp: tự tạo lỗ xốp hoặc hệ nhiều bơm thẩm thấu: NaCl, NaBr, KCl, KHSO4, CaCl2, CaNitrat, manitol, lactose, sorbitol
- Dung môi bao: Dung mỗi hưu cơ như aceton, methanol, ethanol,
- Chất hóa dẻo: PG, triethyl citrat, diethyl tartarat, deiacetin,
- Bào chế viên nhân: Xát hạt ướt hay dập thẳng
- Bao màng bán thấm: bao film, bao nhúng, bao dập
- Tạo miệng giải phóng: Máy khoan cơ học hoặc khoan laser hoặc tá dược tạo lỗ xốp.
Công thức viên nhân (cho 1 viên):
| Tá dược | Khối lượng (mg) |
|---|---|
| Venlafaxin hydroclorid | 86 |
| HPMC K4M | 70 |
| Natri clorid | 20 |
| Manitol | 50 |
| Lactose | 75 |
| Avicel PH 101 | 45 |
| Magnesi stearat | 2 |
| Bột talc | 2 |
| PVP K30 10% trong ethanol 96% | vừa đủ |
Công thức màng bao bán thấm cellulose acetat (Cho 100 viên):
| Tá dược | Khối lượng (g/ml) |
|---|---|
| Opadry® chứa CA/PEG 3350 | 14 g |
| (tỷ lệ 9:1) | 12 g |
| PVP K30 | 6.7 ml |
| Nước tinh khiết | 300 ml |
| Aceton | vừa đủ |
Công thức màng bao bảo vệ (Cho 100 viên):
| Tá dược | Khối lượng (g/ml) |
|---|---|
| HPMC E6 | 10 g |
| PEG 400 | 5 g |
| Câu chuyện | 2 g |
| Titan dioxyd | 1 g |
| Ethanol 70% | 200 ml |
Công thức viên nhân (cho 100 viên):
Hệ thuốc giải phóng
| Tá dược | Khối lượng (g) |
|---|---|
| Glipizid | 4.5 |
| PEG 200,000 | 90 |
| Natri clorid | 15 |
| Lactose | 70 |
| Magnesi stearat | 1.5 |
| Aerosil | 3.5 |
Công thức lớp đây.
| Tá dược | Khối lượng (g) |
|---|---|
| PEG 5,000,000 | 50 |
| Natri clorid | 15 |
| Avicel | 30 |
| Lactose | 25 |
| Sắt oxyd | 0.2 |
| Magnesi stearat | 1.0 |
| Aerosil | 0.5 |
Công thức màng bao bán thâm:
| Tá dược | Khối lượng (g/ml) |
|---|---|
| Cellulose acetat (Opadry CA) | 19.7 g |
| Nước tinh khiết | 9.0 ml |
| Aceton | 420 ml |
(Đường kính lỗ khoan 0.8 mm)
Công thức mảng bao bảo vệ:
| Tá dược | Khối lượng (g/ml) |
|---|---|
| HPMC E6 | 7.14 g |
| Glipizid | 0.5 g |
| PEG4000 | 0.71 g |
| Titan dioxyd | 0.71 g |
| Câu chuyện | vừa đủ |
| Sắt oxyd | 0.71 g |
| Ethanol 96% | 140 ml |
Đánh giá một số tính chất đặc trưng của hệ thuốc
Đánh giá độ hòa tan huặc khả năng khuếch tán giải phóng được chất từ hệ thuốc
Độ hòa tan, khuếch tán giải phóng được chất từ hệ thuộc được đánh giá theo thời gian kéo đài ở các thời điểm (2 giờ, 4 giờ, 6 giờ, 8 giờ, 24 giờ) với các thiết bị và điều kiện thử cụ thể cho từng chế phẩm.
Ví dụ: Viên Clarinase repetabs của Singapore có hàm lượng ghi trên nhân Pseudoephedrin sulfat 120mg (giải phóng kéo dãi) và Loratadin 5mg (có thời gian bán thai 24 giờ) có tiêu chuẩn về độ hòa tan: đối với pseudoephedrin sulfat ≤ 60% sau 1 giờ ở môi trường dịch vị, ≤ 65% sau 2 giờ. ≥ 65% sau 5 giờ, ≥ 80% sau 6 giờ ở mỗi trường dịch ruột so với hàm lượng ghi trên nhân.
Viên Herbesser R200 (Nhật Bản) có tiêu chuẩn thử đỡ hòa tan trong 900 ml nước: 5-30% sau 2 giờ, 25-55% sau 6 giờ, ≥ 85% sau 24 giờ.
Đánh giá so sánh độ hòa tan (sinh khả dụng in vitro) của mẫu thuốc thứ với mẫu đôi chứng
Xác định sự khác nhau và giống nhau giữa 2 mẫu như sau:
Xác định đó hòa tan của 2 mẫu thuốc (thủ và đối chiếu) mỗi mẫu 12 đơn vị.
Từ dữ liệu độ hòa tan tỉnh chỉ số khác nhau (fl) và chỉ số giống nhau (f2) theo công thức:
\[f_1=\frac{\sum^n_{t=1}|R_t-T_t|}{\sum^n_{t=1}R_t}100 \]
\[f_2=50 log(1+\frac{1}{n}\sum^n_{t=1}(R_t - T_t)^2)^{-0.5}100 \] Trong đó: n là số điểm lấy mẫu, Ri là giá trị hóa tan của lô đổi chiếu ở thời gian t và Ti là giá trị độ hòa tan của lô thư ở thời gian t
Hai mẫu được xác định trong cùng điều kiện, các thời điểm lấy mẫu như nhau.
Điểm lây mẫu cuối nên có giá trị độ hòa tan > 85%. Điểm lấy mẫu sớm nhất cho phép có CV < 20%. Ở các thời điểm khác không nên cỏ CV > 10%.
Hai đường cong trong đồ thị độ hòa tan được cho là giống nhau khi fi gần về 0 và f: gần về 100. Thông thường tì từ 0-15 và 12 > 50 đảm bảo sự giống nhau giữa 2 đường cong về độ hòa tan giữa mẫu thử và mẫu đối chiếu.
Đánh giá sinh khả dụng in vivo và tương đương sinh học
Thường dùng phương pháp xác định các thông số được động học (\(C_{max}\) \(T_{max}\).AUC) để đánh giá sinh khả dụng in vivo. Các cơ quan quản lý FDA (Hoa Kỳ) hoặc ASEAN, Châu Âu… đã đưa ra các quy định hướng dẫn cụ thể về các nội dung:
- Lựa chọn đối tượng thủ (động vật, người tình nguyên).
- Chế phẩm đối chiếu, chế phẩm thư.
- Thiết kế nghiên cứu, thời điểm lấy mẫu.
- Thẩm định phương pháp phân tích…
Đánh giá sinh khả dụng
- \(C_{max}\) và \(T_{max}\)
- $AUC_{0-}= AUC_{0-t} + \(C_{tn}/\lambda_z\)$
Đánh giá tương đương sinh học
Nghiên cứu chèo, đơn liễu, hai thuốc, hai giai đoạn, hai trình tự thử thuốc với Cmax. AUC và MRT (số liệu có thể chuyển logarit):
- Phân tích phương sai đánh giá ảnh hưởng của các yếu tố như trình tự, giai đoạn, thuốc, cả thể tới kết qua thư nghiệm.
- Tỉnh khoảng tin cậy 90% của sự chênh lệch giữa giá trị trung bình của thuốc thửvà thuốc đối chiếu. Nếu giới hạn khoảng tin cậy nằm trong khoảng 80-125% thi hai chế phẩm được coi như là tương đương sinh học (khi tỉnh dạng logarit).
- Với Tmux : đánh giá theo phương pháp thống kê phi tham số. Yêu cầu giá trị Tmax của thuốc thử và thuốc đổi chứng sai khác không có ý nghĩa thống kẻ.
Xác định mô hình động học giải phóng được chất từ hệ thuốc
Dựa trên dữ liệu độ hòa tan, đánh giá các số liệu tính theo phương trình toán học của mô hình và của mẫu thực tại các thời điểm. Sau đó căn cứ vào giá trị của các chỉ
Polymer
Polymer
| Type of material | Type of device | Loaded drug | Burst release | Release kinetics | Transport mechanism |
|---|---|---|---|---|---|
| Segmented PU (Cardiomat 610) | Drug-eluting stent | 1,3-Dipropyl-8-cyclopentyl xanthine | 1 d | Near linear release (~ 20 d) | Non-Fickian diffusion |
| Elast-Eon™ | Drug-eluting stent | Dexamethasone acetate | w/ | Biphasic pattern | Fickian diffusion |
| Polyurethane (Walopur®) | Disk-shaped matrices | Flucloxacillin-Na, Fosfomycin, Gentamicin-base | 1 d | Near linear (2 ~ 5 d) | Matrix-controlled |
| Poly(urea-urethane) | Microcapsule | Auramine (Oil-soluble dye) | w/o | Near linear (~20 min) | Non-Fickian Diffusion |
| PEG modified polyurethane | Dermal patch | Thiamazole, diclofenac sodium, ibuprofen | 12 h | Biphasic pattern (~ 48 h) | - |
| PDMS | Rod (matrix vs. reservoir) | Ivermectin | w/o | Matrix: first order, 50 d; Reservoir: zero order, 84 d | Matrix: diffusion, Reservoir: case II transport |
| PDMS | Intravaginal ring (reservoir) | TMC120 | 1–2 d | Biphasic; near zero order release for 30 d | Case II transport |
| PDMS | Intravaginal ring (core-type) | TMC120 | w/o | Zero order, 71 d | Case II transport |
| PDMS | Strip (10×20 mm) | Metronidazole | w/ | Higuchi (linear vs. t1/2) | Fickian diffusion |
| PEVA (VA content, 40%) | Membrane | Quinupramine | w/ | Higuchi (linear vs. t1/2) | Fickian diffusion |
| PEVA | Thin film | Acyclovir, Chlorhexidine diacetate | w/o | Near zero-order (~ 8 d) | Non-Fickian diffusion |
| PEVA | Drug-eluting stent coating | 5-Fluorouracil | w/ | Biphasic pattern (~20 d) | Fickian diffusion |
| PEVA (VA content, 40%) | Disk-shape Film | Chlorhexidine diacetate | w/ | Near-zero order (~ 7 d) | Non-Fickian diffusion |
| PEVA (VA content, 40%) | Membrane | Furosemide | w/ | Higuchi (linear vs. t1/2) | Fickian diffusion |
| Dextran sulfate | Microcapsule | Insulin | w/ | Biphasic pattern (~12 h) | Fickian diffusion |
| Methacrylated dextran | Hydrogel | Vitamin E | ~3 h | Biphasic | Swelling |
| HPMC with β-CD | Tablet | Difunisal | w/o | Zero-order for nonsoluble β-CD; First-order for soluble β-CD | Non-Fickian diffusion |
| Type of material | Type of device | Loaded drug | Burst release | Release kinetics | Transport mechanism |
|---|---|---|---|---|---|
| PLGA/PLA | Microparticle | Diltiazem hydrochloride | 2h | Triphasic pattern | Diffusion and erosion |
| PLGA | Nanoparticle | Estradiol | w/o | Zero order up to 31 ~54 d | Diffusion-cum-degradation |
| PLGA | Microcapsule | Insulin | 20%, 24h | Triphasic pattern | Diffusion and erosion |
| p(FAD-SA) 50:50 | Implantable disk | Cefazolin sodium | w/o | 100%, 14 d | Diffusion |
| Bupivacaine free base | w/o | 90%, 35 d | Diffusion and degradation | ||
| Taxol | w/o | 15%, 77d | Degradation | ||
| PEG hydrogel with degradable crosslinks | Disk | Bovine serum albumin | w/o | Zero order in the presence of human neutrophil elastase | Triggered degradation |
| Poly(ortho ester amide) copolymer | NA | FITC-dextran | w/o | Near zero order | Erosion |
| HPMC | Tablet | Adinazolam mesylate | w/ | Near zero order, 10h | Swelling and dissolution |
Câu hỏi lượng giá
Lượng giá
Hãy dành 15 phút để tìm hiểu vấn đề xung quanh. 02 bạn lên phân tích.
- Phân tích ưu nhược điểm của hệ thuốc giải phóng kéo dài với thuốc quy ước dựa trên cơ sở phân tích đặc điểm giải phóng dược chất.
https://dainam.edu.vn